Teoría y medición de pH
El sistema de medición de pH comúnmente utiliza electrodos de vidrio. El sistema consiste en un electrodo indicador (cuyo voltaje varía proporcionalmente a la actividad del ion hidrógeno de la solución), un electrodo de referencia (que proporciona un voltaje estable de referencia), una solución electrolito y un instrumento específico para medir y mostrar el valor del pH.
El instrumento mide la diferencia de voltaje entre el electrodo indicador y el de referencia en milivoltios de corriente continua (mV DC). La medición es interpretada por el instrumento y mostrada ya sea en unidades de mV o pH. La respuesta en mV de un electrodo de pH sigue la ecuación de Nernst:
)
Eobs = Potencial observado
Ec = Potencial de referencia, incluyendo otros potenciales estables y fijos
aH+ = Actividad del ion hidrógeno
T = Temperatura en Kelvin (°C + 273,15)
n = valencia del ion medido (1)
F = Constante de Faraday (9,6485 × 10⁴ C/mol)
R = Constante de los gases (8,31432 J/(K·mol))
A partir de esta ecuación se puede observar que, si la temperatura (T) cambia, el término ln(10)RT / nF, conocido como factor de pendiente, también cambiará. La tabla a continuación ilustra la variación del factor de pendiente debido a cambios en la temperatura.
Efecto de la temperatura sobre el factor de pendiente en pH
La pendiente del electrodo representa la variación de potencial (mV) que genera un electrodo por cada unidad de pH. De acuerdo con la ecuación de Nernst, esta pendiente aumenta proporcionalmente con la temperatura.
A 25 °C, el valor teórico es 59,16 mV/pH, considerado el estándar de calibración.
Cuando la temperatura se aleja de este valor, la respuesta del electrodo cambia, como se observa en la tabla:
| Temperatura (°C) | Factor de pendiente (mV/pH) |
| 5 | 55,18 |
| 10 | 56,18 |
| 15 | 57,18 |
| 20 | 58,17 |
| 25 | 59,16 |
| 30 | 60,15 |
| 35 | 61,14 |
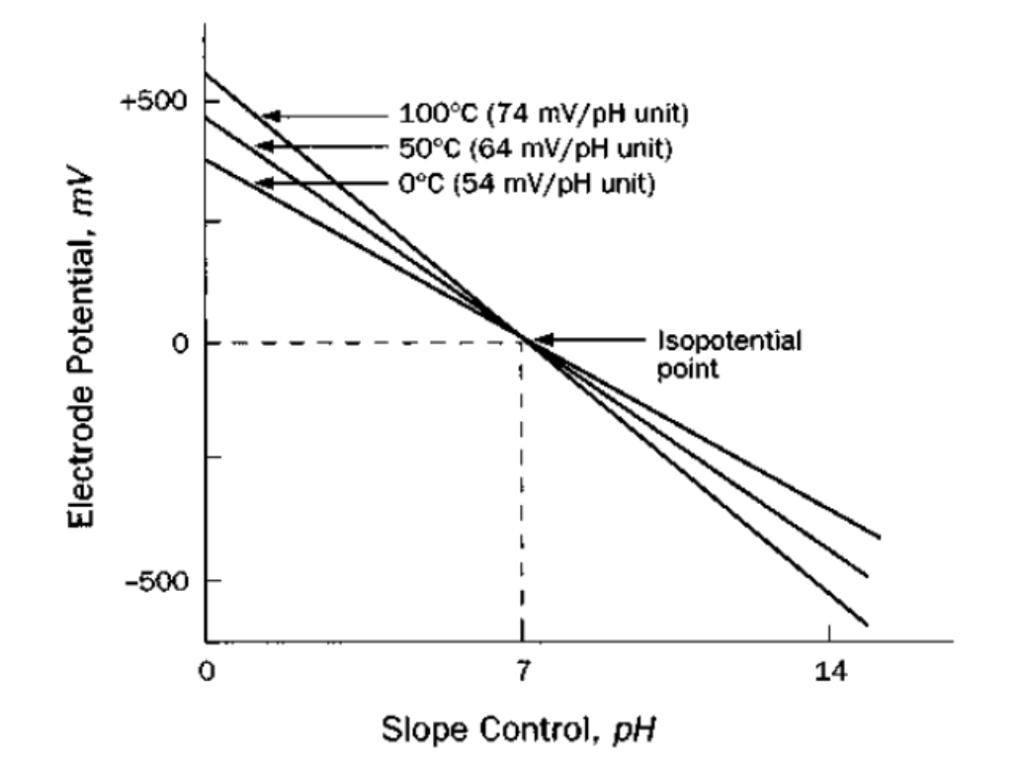
Figura 1. Respuesta típica del electrodo de pH en función de la temperatura
Cómo la temperatura afecta el pH de las soluciones
Las muestras cambian su pH en función de la temperatura debido a las variaciones en la disociación iónica; a medida que la temperatura aumenta, también aumenta la actividad iónica. Un ejemplo de esto son los buffers de pH, cuyos valores están bien caracterizados y se encuentran publicados en las etiquetas de los frascos.
Todas las muestras poseen un coeficiente de temperatura que varía según sus características específicas. Los cambios en el pH debidos al coeficiente de temperatura de la muestra no son compensados por el instrumento. No obstante, existe una excepción: dado que los buffers están bien caracterizados, sí son compensados durante la calibración en medidores de pH inteligentes. Los buffers mostrarán su valor a 25 °C durante la calibración, pero después de esta, el valor visualizado cambiará para reflejar el pH real a la temperatura de medición.
Entradas de temperatura
Ya que la temperatura afecta las mediciones de pH, se requiere compensación de temperatura para obtener resultados precisos. La compensación de temperatura puede lograrse de tres maneras:
Una sonda independiente diseñada específicamente para medir temperatura.
Una sonda con sensor de temperatura incorporado.
Ajuste manual de la temperatura.
Si no se dispone de una entrada de temperatura, muchos instrumentos aún ofrecen la capacidad de ajustar manualmente la temperatura.
Compensación de temperatura en pH
Las lecturas de pH deben ser compensadas por temperatura para asegurar resultados exactos. La compensación en pH proporciona el valor real de pH a la temperatura en la que se realiza la medición.
Durante la calibración, los buffers de pH reconocidos son compensados por temperatura por el instrumento con el fin de considerar la variación del pH de estas soluciones debido al cambio de la temperatura. Por ejemplo, un buffer de pH 10.01 tiene ese valor únicamente a 25 °C. La tabla con la variación del pH en función de la temperatura se encuentra impresa en la etiqueta de cada buffer de pH.
Sebastián Pinzón.
Ingeniero de Aplicaciones
(+57) 318 889 56 08








